
Tecniche di procreazione medicalmente assistita (PMA)
Dal momento in cui una coppia, dopo 12 mesi di regolari rapporti sessuali non protetti, non ottiene una gravidanza, è bene che si rivolga ad uno specialista di medicina della riproduzione per ulteriori approfondimenti ed eventualmente, ricorrere ad una tecnica di fecondazione assistita. Le tecniche di fecondazione assistita possono essere distinte in base al loro grado di invasività in tecniche di primo livello e tecniche di II e III livello.
Tecniche di I livello
 L’inseminazione intrauterina (IUI) è la tecnica più semplice di Procreazione Medicalmente Assistita che consiste nella preparazione del liquido seminale del partner maschile in laboratorio secondo specifici protocolli che ne migliorano le caratteristiche e permettono di selezionare gli spermatozoi più mobili per poi depositarli in cavità uterina con un apposito catetere, al fine di incrementare la densità di gameti nel sito dove avviene in vivo la fecondazione. La tecnica viene effettuata quando il ginecologo ritiene sia il momento più opportuno, ovvero in prossimità dell’ovulazione, valutata sottoponendo la paziente a monitoraggi follicolari costanti fino all’ovulazione e, in alcuni casi, combinando una lieve stimolazione farmacologica e induzione dell’ovulazione mediante l’utilizzo di farmaci. Una volta deciso il giorno in cui effettuare la tecnica, al partner maschile viene richiesto di effettuare la raccolta del liquido seminale e, dopo essere stato processato dal personale di laboratorio, il ginecologo lo introdurrà all’interno della cavità uterina della donna mediante un sottile catetere.
L’inseminazione intrauterina (IUI) è la tecnica più semplice di Procreazione Medicalmente Assistita che consiste nella preparazione del liquido seminale del partner maschile in laboratorio secondo specifici protocolli che ne migliorano le caratteristiche e permettono di selezionare gli spermatozoi più mobili per poi depositarli in cavità uterina con un apposito catetere, al fine di incrementare la densità di gameti nel sito dove avviene in vivo la fecondazione. La tecnica viene effettuata quando il ginecologo ritiene sia il momento più opportuno, ovvero in prossimità dell’ovulazione, valutata sottoponendo la paziente a monitoraggi follicolari costanti fino all’ovulazione e, in alcuni casi, combinando una lieve stimolazione farmacologica e induzione dell’ovulazione mediante l’utilizzo di farmaci. Una volta deciso il giorno in cui effettuare la tecnica, al partner maschile viene richiesto di effettuare la raccolta del liquido seminale e, dopo essere stato processato dal personale di laboratorio, il ginecologo lo introdurrà all’interno della cavità uterina della donna mediante un sottile catetere.
La IUI è indicata in molteplici casi quali disfunzione erettile, eiaculazione retrograda, vaginismo, impotenza, fattore maschile lieve e comunque in tutti quei casi in cui non si è ottenuta una gravidanza dopo 12 mesi di rapporti non protetti senza aver trovato alcuna apparente causa di infertilità (infertilità idiopatica o sine causa) come primo approccio alla procreazione medicalmente assistita. Condizione imprescindibile per effettuare l’inseminazione intrauterina è l’assenza d’impedimenti strutturali a livello tubarico che potrebbero impedire il raggiungimento degli ovociti da parte degli spermatozoi (pervietà tubarica).
Tecniche di II livello
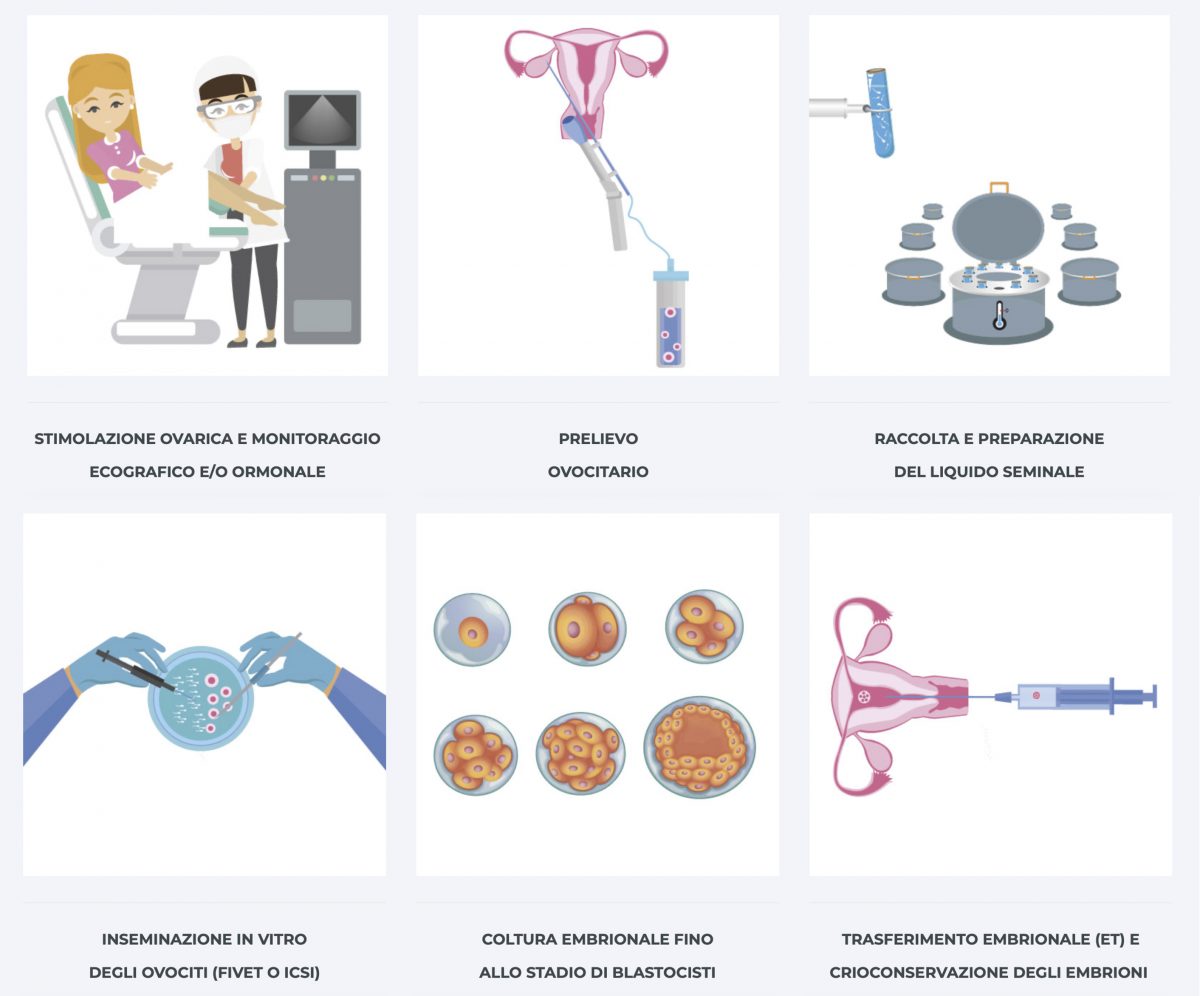
Le tecniche di secondo livello (spesso conosciute come FIVET, acronimo di Fecondazione in Vitro con Embryo Transfer o ICSI, acronimo di Intra Cytoplasmic Sperm Injection o iniezione intracitoplasmatica dello spermatozoo) vengono proposte quando precedenti terapie mediche o approcci di primo livello non abbiano avuto successo o, comunque, quando rappresentano l’unico trattamento possibile. In entrambe i casi, l’iter di preparazione della coppia prevede le seguenti fasi:
STEP1 – Stimolazione ovarica controllata e Induzione dell’ovulazione
Al fine di ottenere il maggior numero di ovociti per la fecondazione assistita, le pazienti vengono sottoposte ad una stimolazione ovarica controllata mediante l’utilizzo di gonadotropine in modo da indurre una crescita follicolare multipla e cercare di recuperare un numero di ovociti superiore all’unico normalmente prodotto in un ciclo spontaneo in modo da aumentare le probabilità di successo della paziente. Durante la stimolazione la paziente viene sottoposta a controlli diversi ecografici, ai quali possono essere associati prelievi di sangue al fine di valutare i livelli serici di alcuni ormoni come gli estrogeni per monitorare la crescita follicolare.
Solitamente, quando i follicoli hanno raggiunto un diametro di circa di 18 mm ed il valore di estrogeni risulta adeguato rispetto al numero di follicoli presenti, si procede con l’induzione dell’ovulazione mediante la somministrazione di un ormone chiamato gonadrotopina corionica umana (HCG) e successivamente con il prelievo ovocitario.
STEP2 – Prelievo ovocitario (PICK_UP)
Il prelievo ovocitario viene effettuato all’incirca 34-36 ore dalla somministrazione della gonadotropina corionica umana, in sala operatoria ed in sedazione. Mediante un sottile ago e per via trans-vaginale, il ginecologo aspira il fluido contenuto nei follicoli formatisi durante la stimolazione all’interno di provette che vengono immediatamente consegnate in laboratorio. Sotto cappa, il biologo analizza il contenuto delle provette, individua gli ovociti, li recupera e li trasferisce in provette/piastre contenenti un adeguato terreno di coltura per poi riporli all’interno di un incubatore in attesa dell’inseminazione.
STEP3 – Preparazione del liquido seminale
Sia nel caso di ICSI che di fecondazione in vitro classica FIV, al partner maschile viene richiesto di effettuare la raccolta del liquido seminale che verrà poi processato dal personale di laboratorio secondo lo stesso protocollo già descritto per la IUI e diluendolo nel volume opportuno, idoneo alla tecnica prescelta (FIV o ICSI).
STEP4 – Fecondazione degli ovociti
- FIV – Fecondazione in vitro. Nella FIV la fecondazione avviene mediante selezione naturale, simile a ciò che avviene in condizioni fisiologiche ma con il vantaggio di facilitare l’incontro ovocita-spermatozoo. Una volta che gli ovociti sono stati recuperati al pick-up, trascorso un breve periodo in incubazione, vengono trasferiti ancora circondati dalle cellule del cumulo ooforo in una piastra contenente il terreno di coltura appropriato e messi a diretto contatto con gli spermatozoi opportunamente preparati per la tecnica. Ovviamente, perché sia possibile effettuare una FIV è necessario che liquido seminale abbia delle buone caratteristiche in motilità e morfologia, e che il numero sia tale da poter ottenere una concentrazione di spermatozoi mobili adeguata.
- ICSI- Iniezione intracitoplasmatica dello spermatozoo. La ICSI consiste nell’iniettare direttamente all’interno dell’ovocita un singolo spermatozoo mediante un microscopio invertito allestito con uno strumento chiamato micromanipolatore che consente di effettuare spostamenti microscopici nelle tre dimensioni. La tecnica è stata messa appunto dal ricercatore Italiano Giampiero Palermo nel 1992 per risolvere tutti quei casi di infertilità da fattore maschile laddove non c’era la possibilità di effettuare una FIV classica (es. spermatozoi di scarsa qualità o immobili, e/o recuperati chirurgicamente dai testicoli dei pazienti). Una volta che gli ovociti sono stati recuperati al pick-up, trascorso un breve periodo in incubazione, vengono denudati dalle cellule del cumulo ooforo che lo circondano e solo quelli maturi, definiti come metafase II (MII) vengono inseminati, mentre quelli immaturi (metafase I, MI o vescicola germinale, VG) vengono valutati come non idonei e scartati.
STEP5 – Il controllo dell’avvenuta fecondazione e la coltura embrionale
I segni dell’avvenuta fecondazione vengono visualizzati dopo 16-18 ore dall’inseminazione degli ovociti visualizzando all’interno della cellula fecondata (zigote) la presenza di due pronuclei che portano rispettivamente l’informazione genetica di origine materna e paterna. In seguito alla fusione dei due pronuclei, s’innesca una cascata di eventi molecolari e cellulari che porterà alla formazione dell’embrione e al suo conseguente sviluppo. Il giorno successivo alla fertilizzazione l’embrione è solitamente allo stadio di 4 cellule (giorno 2) per poi raggiungere lo stadio di 8 cellule al giorno 3, diventare una morula al giorno 4 e, infine, una blastocisti tra il giorno 5-7 di coltura embrionale. Durante questo periodo di sviluppo gli embrioni sono mantenuti in coltura in sistemi ottimizzati per riprodurre al meglio le condizioni naturali dell’ambiente uterino e mantenere più indisturbate possibili le condizioni di coltura, ad una concentrazione di CO2 e O2 controllata (circa 5-6% per entrambe i parametri). Una volta ottenuti gli embrioni/blastocisti, questi possono essere:
- trasferite (nel caso di ciclo fresco);
- analizzate da un punto di vista genetico effettuando il test genetico preimpianto (PGT- Preimplantation Genetic Testing) mediante biopsia del trofoectoderma della blastocisti per vedere se ci sono problematiche nel numero dei cromosomi (PGT-A), nella loro struttura (PGT-SR) oppure genetiche (PGT-M) e poi trasferite su ciclo differito.
- crioconservate e poi trasferite su ciclo differito .
STEP6 – Il Trasferimento degli embrioni
Il trasferimento degli embrioni, ET acronimo di embryo transfer, può essere effettuato dalle dal giorno 2 al giorno 5-6 dal prelievo ovocitario. Il numero di embrioni da trasferire, così come la scelta del giorno in cui effettuare il transfer, dipende da molte variabili e la strategia da seguire viene solitamente concordata con il medico responsabile del trattamento e con l’embriologo. La procedura del transfer embrionario è ambulatoriale e consiste nell’inserire gli embrioni formatisi all’interno della cavità uterina tramite un sottile catetere nel quale il biologo ha precedentemente caricato gli embrioni scelti. Dopo di che, la paziente seguirà una terapia ormonale specifica per la fase luteale prescritta dal medico e circa 13-15 giorni dal pick-up effettuerà il test di gravidanza (dosaggio serico della βhCG) per appurare l’esito del trattamento.
Il congelamento ovocitario ed embrionale
 Gli ovociti e gli embrioni/blastocisti possono essere crioconservati mediante una tecnica chiamata “vitrificazione”. Si tratta di una metodica che consente di conservarli in azoto liquido a bassissime temperature (-196°C) senza procurargli alcun danno da raffreddamento (lesioni da cristalli di ghiaccio) anche per lunghissimi periodi di tempo. La vitrificazione, infatti, non compromette in alcun modo la competenza ovocitaria o il potenziale riproduttivo degli embrioni.
Gli ovociti e gli embrioni/blastocisti possono essere crioconservati mediante una tecnica chiamata “vitrificazione”. Si tratta di una metodica che consente di conservarli in azoto liquido a bassissime temperature (-196°C) senza procurargli alcun danno da raffreddamento (lesioni da cristalli di ghiaccio) anche per lunghissimi periodi di tempo. La vitrificazione, infatti, non compromette in alcun modo la competenza ovocitaria o il potenziale riproduttivo degli embrioni.
La crioconservazione degli ovociti può essere necessaria:
- in caso di iperstimolo della paziente,
- qualora il partner sia stato impossibilitato a fornire il campione di liquido seminale
- in caso non siano rinvenuti spermatozoi nel liquido seminale per cui non è possibile procedere con l’inseminazione degli ovociti.
La crioconservazione degli embrioni può essere necessaria:
- in caso di test genetico preimpianto, in attesa del referto dal laboratorio di genetica;
- qualora il trasferimento nell’utero degli embrioni non risulti possibile per grave e documentata causa di forza maggiore, relativa allo stato di salute della donna (es. in caso di sindrome da iperstimolazione ovarica);
- in caso di asincronia endometriale;
- in caso di eventuali embrioni soprannumerari.
Tecniche di III livello
Recupero chirurgico degli spermatozoi
In alcuni casi il liquido seminale, prodotto finale della secrezione di una serie di ghiandole accessorie dell’apparato genitale maschile, può essere privo di spermatozoi, una problematica nota con il nome di azoospermia che può essere distinta in: ostruttiva, se è presente un impedimento meccanico alla loro emissione, non-ostruttiva o secretiva, quando è dovuta ad un’alterazione della spermatogenesi e/o a cause genetiche. In pazienti con azoospermia ostruttiva è possibile recuperare gli spermatozoi a livello dell’epididimo tramite due tipologie di tecniche di III livello, la MESA (Microsurgical Epididimal Sperm Aspiration) o la PESA (Percutaneus Epididimal Sperm Aspiration). Nel caso in cui le metodiche precedentemente citate non abbiamo dato esito o l’azoospermia sia di tipo secretivo, per i quali è impossibile reperire spermatozoi nell’epididimo, è possibile il recupero diretto dal testicolo tramite due tipologie di tecniche di III livello, l’FNA (Fine Needle Aspiration) o la TESE (Testicular sperm Estraction).
IL TEST GENETICO PREIMPIANTO (PGT)

La PGT è un test che consente di analizzare i cromosomi di un embrione mediante l’analisi genetica di alcune delle sue cellule. È indicata nei seguenti casi:
- Quando un partner è affetto o entrambe i partners sono portatori di malattie genetiche ereditare come fibrosi cistica, beta talassemia etc. e in questo caso prende il nome di PGT-M.
- Quando uno o entrambe i partners sono portatori di anomalie strutturali dei cromosomi come inversioni, traslocazioni e in questo caso prende il nome di PGT-SR.
- Quando si vuole conoscere lo stato di salute dell’embrione e, in particolare, se presenta anomalie nel numero dei cromosomi definite aneuploidie spesso responsabili di ripetuti fallimenti, aborti e correlati ad un età materna avanzata es. monosomie, trisomie come la trisomia 21 (Sindrome di Down), trisomia 18 (sindrome di Edwards) etc., e in questo caso prende il nome di PGT-A.
Il test si effettua previa biopsia (prelievo) di alcune cellule del trofoectoderma (TE) della blastocisti, la porzione di cellule più esterne della blastocisti che daranno origine agli annessi embrionali (placenta, amnios, corion), senza andare a prelevare le cellule della massa interna (ICM) che sono invece quelle che daranno origine all’embrione. È una villocentesi effettuata allo stadio embrionale di 5, 6, 7 giornata, anziché all’11 settimana, stadio in cui solitamente di effettua la villocentesi in gravidanza (biopsia dei villi coriali). E’ importante ricordare che la PGT non può aumentare le probabilità di successo di una PMA ma solo minimizzare i rischi di aborto, i rischio di avere un bambino affetto da sindromi legate ai cromosomi (es. sindrome di Down) e ridurre il tempo per l’ottenimento della gravidanza (evitando il trasferimento di embrioni che darebbero dei test di gravidanza negativi, oppure, test positivi ma aborti spontanei etc.) identificando prima l’eventuale presenza di un embrione con maggiori potenzialità all’impianto.
